화이자에 이어 두번째 정식 승인…18세 이상
‘오미크론 임상 데이터 없다’는 지적에는 침묵
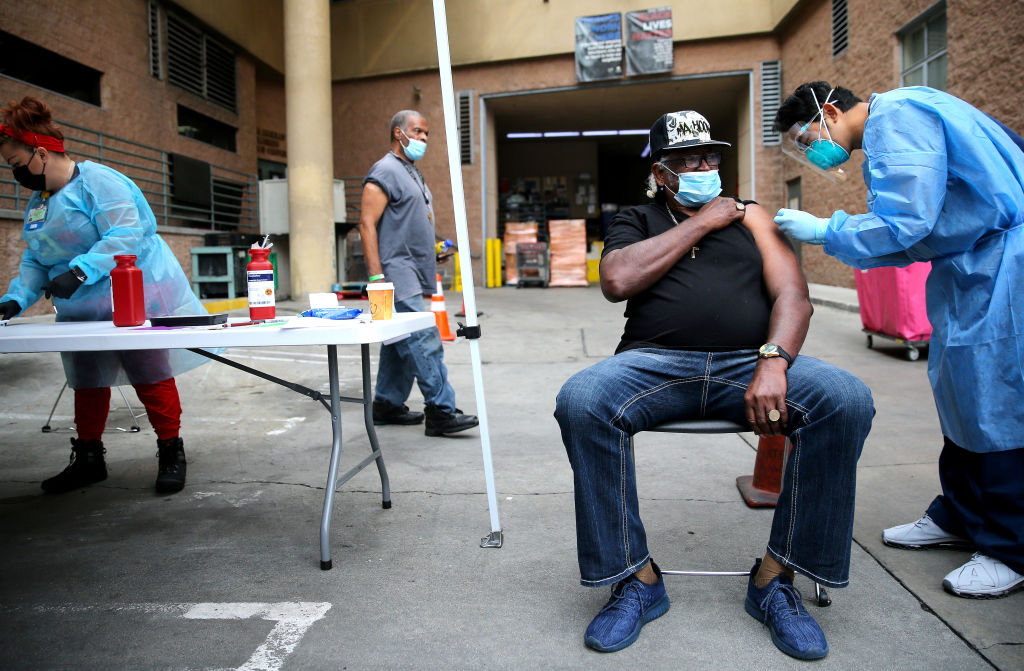
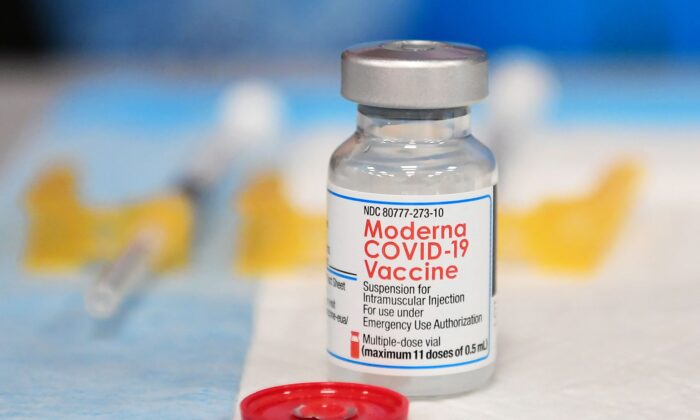
미국 식품의약국(FDA)이 제약사 모더나가 개발한 중공 바이러스 감염증(코로나19) 백신을 정식 승인했다.
FDA는 31일(현지시간) 보도자료를 내고 “(미국에서) 두 번째 코로나19 백신을 승인했다”며 ‘스파이크 백스’라는 제품명으로 판매될 이 백신은 모든 18세 이상을 대상으로 사용될 수 있다고 밝혔다.
FDA는 데이터 분석 결과 이 백신이 중공 바이러스 예방에 93%, 중증 질환 예방에 98% 효과가 있다고 밝혔지만 해당 데이터는 오미크론 변이가 등장하기 이전에 수집된 것이다.
각국에서 발표된 최근 연구결과와 실제 데이터에 따르면 오미크론은 화이자, 모더나, 얀센(존슨앤드존슨) 등 미국에서 사용되는 3종 백신의 보호를 회피해 접종자를 감염시키는 것으로 나타났다.
FDA의 이번 승인에 대한 전문가들의 평가는 엇갈렸다.
베일러대학 의학센터 심장의학 전문의 피터 맥컬로 박사는 “이번 승인이 임상적으로 정당화되거나 임상 데이터에 의해 뒷받침되지 않았다”고 말했다.
맥컬로 박사는 에포크타임스와의 이메일 인터뷰에서 “오미크론 환자에 대한 대규모 무작위 임상실험이 필요하다”며 “백신 승인 전 접종에 따른 이익과 위험성에 대한 판단이 필요하다”고 지적했다.
예일대 공중보건대학 감염병학 하비 리쉬 교수는 “FDA는 사라지고 있는 델타가 아니라 오미크론과 관련한 증거를 (모더나에) 요구했어야 했다”고 지적했다.
버팔로대학 제이콥스의대 감염병 전문가 토마스 루소 박사는 이 같은 견해에 동의하지 않았다.
루소 박사는 “모더나는 자사 백신의 상당한 효능과 안전성을 입증하는 방대한 데이터를 확보했다”며 “시간이 오래 걸렸다는 점이 놀랍지만, FDA가 꼼꼼하게 확인을 한 것 같다”고 말했다.
FDA는 이번 승인에 대해 “1만5천명의 백신 접종자를 대상으로 실시된 3상 임상을 포함해 모든 임상데이터를 분석했다”고 설명했다.
FDA 대변인은 그러나 오미크론 확산 이후 데이터가 포함되지 않은 이유와 모더나 백신의 오미크론 감염 보호효능에 대한 우려를 묻는 질문에는 응답하지 않았다.
모더나 정식 승인은 한 달 간격을 두고 2회 접종하는 1,2차 접종만 해당한다. 소위 ‘부스터샷’으로 불리는 3차 접종은 제외된다.
오미크론에 관한 연구에 따르면, 모더나 1,2차 접종은 오미크론 감염 예방에 별 효능을 보이지 않는다.
미 질병통제예방센터(CDC)는 2차 접종 후 5개월째에 3차 접종을 받도록 권고하고 있다.
이번 정식 승인은 모더나가 작년 8월 정식 승인 절차를 완료한 지 약 5개월 만이다. 지난 2020년 12월 긴급사용 승인 이후로는 약 14개월이 걸렸다.
앞서 작년 8월에는 화이자 백신 ‘코미니티’가 미국에서 첫 번째로 FDA 정식 승인을 받았다.





![트럼프를 ‘악당’으로 만들다…악의적 프레임의 수혜자는 누구? [ATL]](https://kr.theepochtimes.com/assets/uploads/2024/04/rrrr-235x132.jpg)